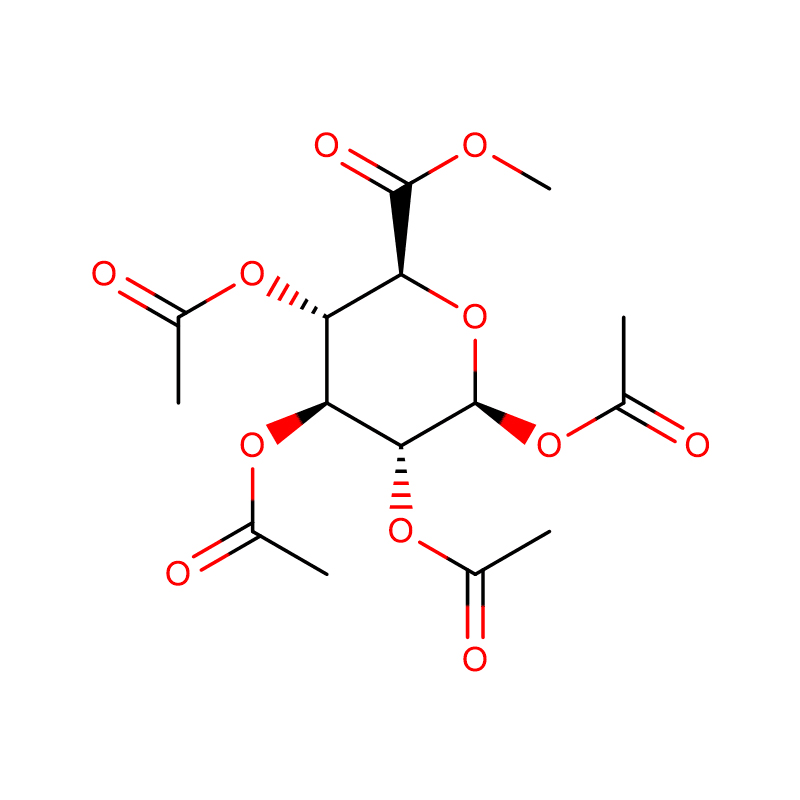
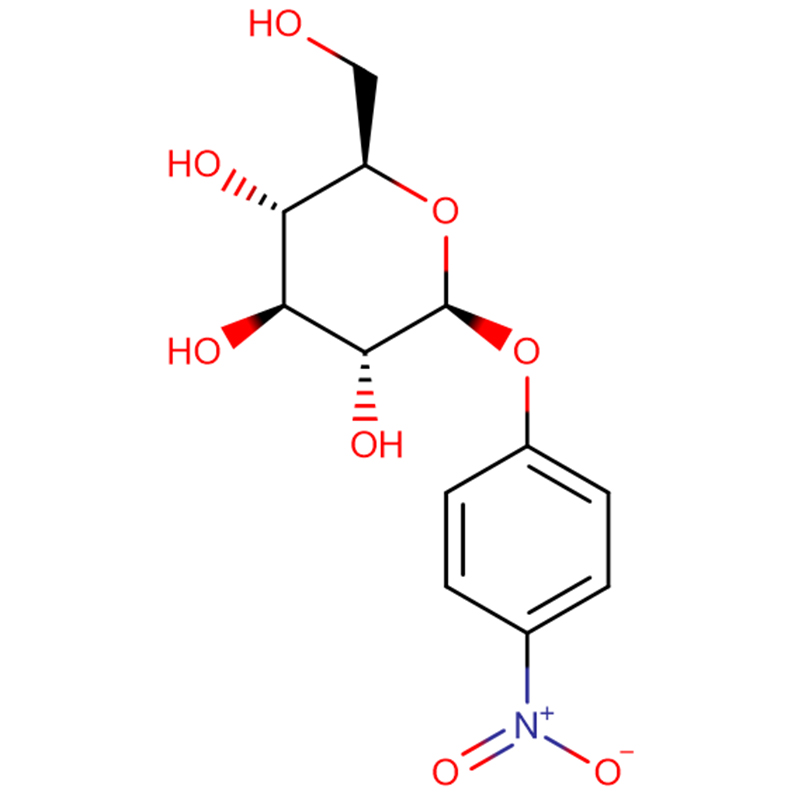
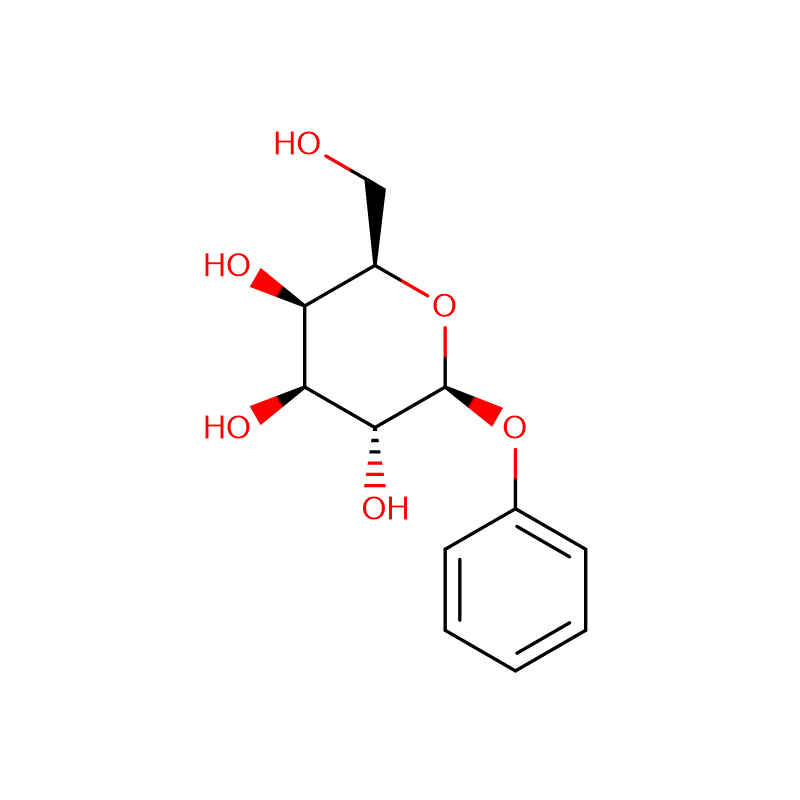
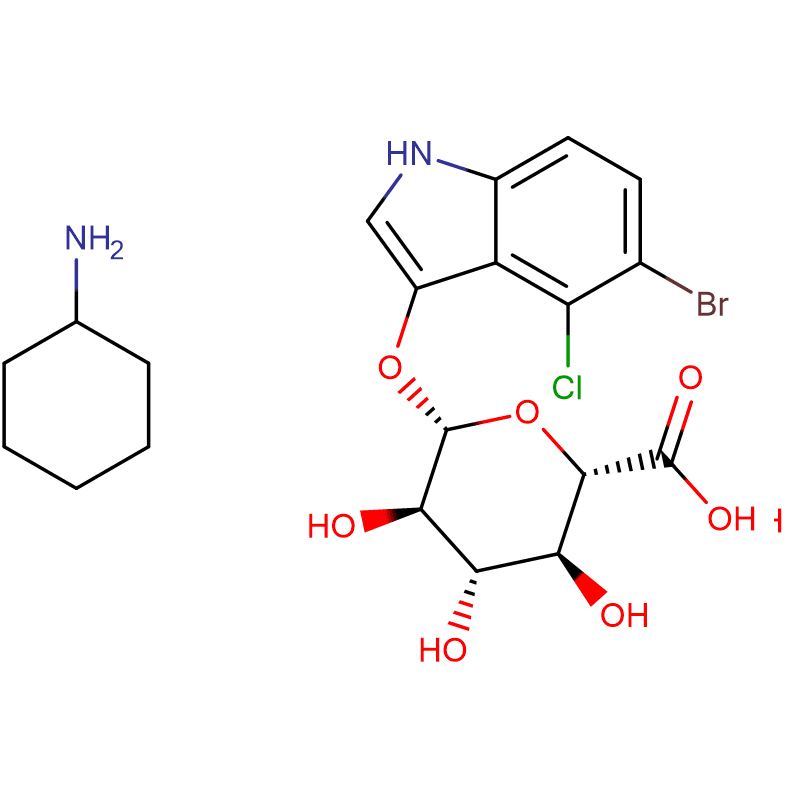
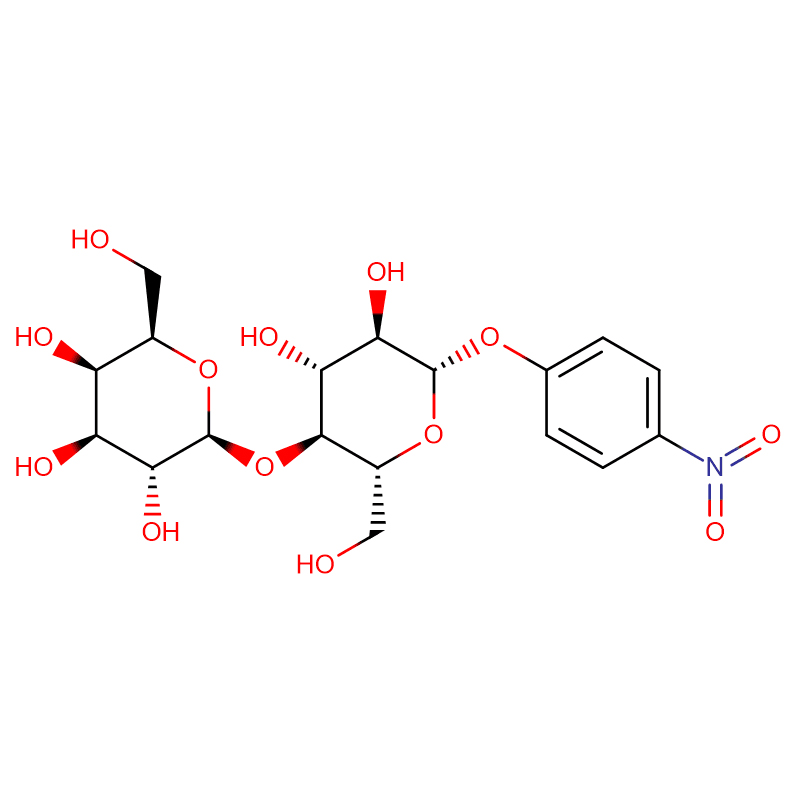
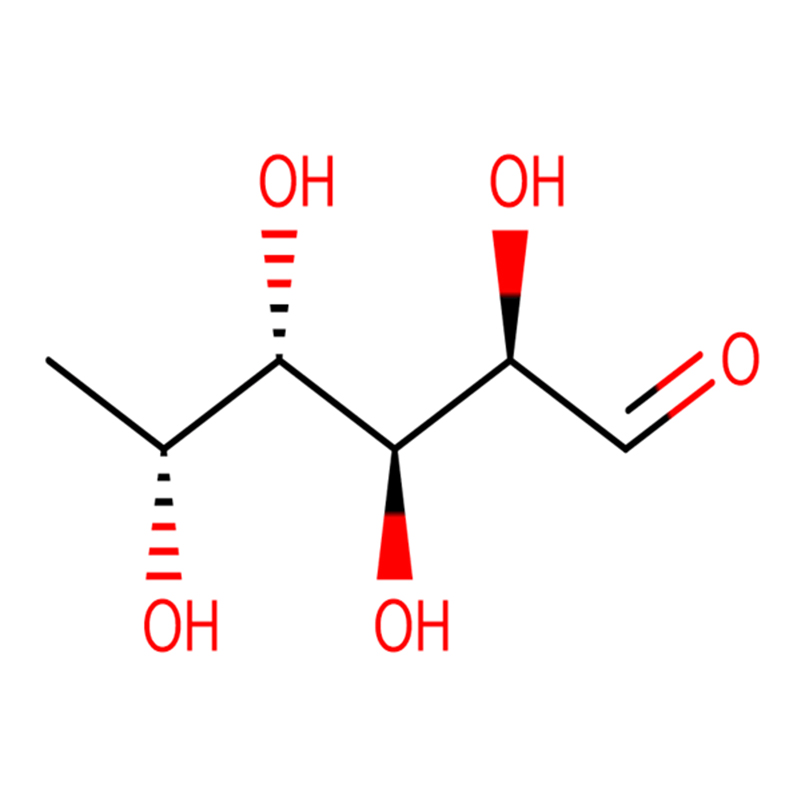
Du izomeraj biciclo[4.1.0]heptananalogoj de la glikosidasa inhibitoro galakto-validamino, (1R*,2S,3S,4S,5S,6S*)-5-amino-1-(hidroksimetil)biciklo[4.1.0]heptano -2,3,4-triol, estis sintezitaj en 13 paŝoj el 2,3,4,6-tetra-O-benzil-D-galaktozo.La inhibiciaj agadoj de la du konformige limigitaj aminoj, kaj iliaj ekvivalentaj acetamidoj, estis mezuritaj kontraŭ komercaj alfa-galaktosidase-enzimoj de kafsebo kaj E. coli.La agado de la glikosil-hidrolaza familio GH27-enzimo (kafo-fabo) estis konkurencive malhelpita per la 1R,6S-amino (7), liga interago kiu estis karakterizita per K(i) valoro de 0.541 microM.La GH36 E. coli alfa-galaktosidase elmontris multe pli malfortan ligan interagadon kun la 1R,6S-amino (IC(50)= 80 microM).La diastereomera 1S,6R-amino (9) ligis malforte al ambaŭ galaktosidases, (kafofabo, IC(50)= 286 microM) kaj (E. coli, IC(50)= 2.46 mM).